Ligações Químicas
As ligações químicas correspondem à união dos átomos para a formação das substâncias químicas.
Os átomos se ligam para buscar estabilidade eletrônica. Segundo a teoria do octeto, a maioria do átomos (excetos H e He) se estabilizam com 8 elétrons em sua ultima camada.
Os principais tipos de ligações são:
Ligações iônicas: transferência de elétrons;
Ligações covalentes: compartilhamento de elétrons;
Ligações metálicas: existência de elétrons livres.
Ligação Iônica
Também chamada de ligação eletrovalente, esse tipo de ligação é realizada entre íons (cátions + e ânions -), daí o termo "ligação iônica".
Para ocorrer uma ligação iônica os átomos envolvidos apresentam tendências opostas: um átomo deve ter a capacidade de perder elétrons enquanto o outro tende a recebê-los.
Portanto, um ânion, de carga negativa, se une com um cátion, de carga positiva, formando um composto iônico por meio da interação eletrostática existente entre eles.
Exemplo: Na+Cl- = NaCl (cloreto de sódio ou sal de cozinha). Nesse composto, o sódio (Na) doa um elétron para o cloro (Cl) e se torna um cátion (carga positiva), enquanto o cloro torna-se um ânion (carga negativa).
Outros exemplos de substâncias formadas por ligações iônicas são:
- Brometo de potássio, KBr
- Cloreto de cálcio, CaCl2
- Fluoreto de magnésio, MgF2
Ligação Covalente ou Molecular
Também chamada de ligação molecular, as ligações covalentes são ligações em que ocorre o compartilhamento de elétrons para a formação de moléculas estáveis, segundo a Teoria do Octeto; diferentemente das ligações iônicas em que há perda ou ganho de elétrons.
Além disso, pares eletrônicos é o nome dado aos elétrons cedidos por cada um dos núcleos, figurando o compartilhamento dos elétrons das ligações covalentes.
Exemplo: H2O: H - O - H (molécula de água) formada por dois átomos de hidrogênio e um de oxigênio. Cada traço corresponde a um par de elétrons compartilhado formando um molécula neutra, uma vez que não há perda nem ganho de elétrons nesse tipo de ligação.
Outros exemplos de substâncias formadas por ligações covalentes são:
- Gás oxigênio, O2
- Sacarose (açúcar de mesa), C12H22O11
- Ácido clorídrico, HCl
As ligações covalentes podem ser classificadas em polares ou apolares. No caso da água temos uma ligação covalente polar, pois os átomos que compõem a molécula apresentam diferentes eletronegatividades. Já o oxigênio (O2) apresenta uma ligação covalente apolar, pois é formado por átomos de um único elemento químico e, por isso, não apresenta diferença de eletronegatividade.
Ligação Metálica
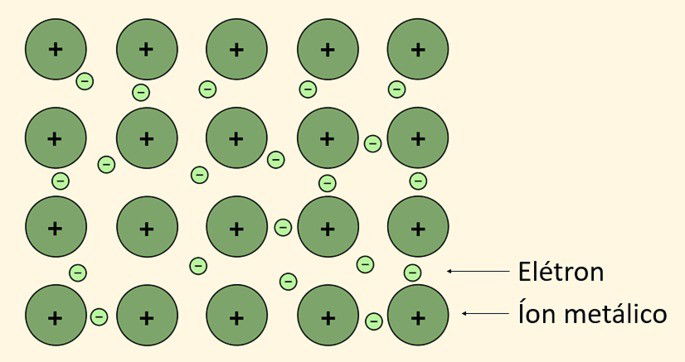
É a ligação que ocorre entre os metais, elementos considerados eletropositivos e bons condutores térmico e elétrico. Para tanto, alguns metais perdem elétrons da sua última camada chamados de "elétrons livres" formando assim, os cátions.
A partir disso, os elétrons liberados na ligação metálica formam uma "nuvem eletrônica", também chamada de "mar de elétrons" que produz uma força fazendo com que os átomos do metal permaneçam unidos.
Exemplos de metais: Ouro (Au), Cobre (Cu), Prata (Ag), Ferro (Fe), Níquel (Ni), Alumínio (Al), Chumbo (Pb), Zinco (Zn), entre outros.
Os metais apresentam estado físico sólido em temperatura ambiente, com exceção do mercúrio, o único metal líquido nessas condições. As substâncias metálicas são boas condutoras de calor e eletricidade e, além disso, apresentam um brilho característico.
Agora assistam ao vídeo resumindo os tipos de ligações químicas:
Valeu!!
Profº Ednei










Daniela da Silva Souza
ResponderExcluirZaqueu Souza Conceicao
ResponderExcluirDaniela Freitas De Oliveira
ResponderExcluirRafael Silva Queiroz
ResponderExcluirPaulo Henrique Jesus de Souza
ResponderExcluirNatiele de Jesus Silva
ResponderExcluirRobert Barbosa de souza
ResponderExcluirVanessa de Jesus Souza
ResponderExcluirMarivania Santos
ResponderExcluirKeliane silva de jesus
ResponderExcluirSamuell Paixão🐊❤️
ResponderExcluirCamila barbosa da paixão
ResponderExcluirjosé carlos da c. neri
ResponderExcluirFlávio Santos De Jesus
ResponderExcluirBeatriz Pereira Silva
ResponderExcluirDaniela da Silva Souza
ResponderExcluirErica Brandão Nery
ResponderExcluirJerfeson Santos Gonçalves ✨
ResponderExcluirVanessa Sena de Jesus
ResponderExcluirRaissa de J Faleiro
ResponderExcluirRaissa de J Faleiro
ResponderExcluirPoliana Barbosa dos santos
ResponderExcluirJosé Carlos da c. neri
ResponderExcluirDaiane Almeida Teixeira
ResponderExcluirJamile de Jesus pereira
ResponderExcluirQueliane Almeida de Jesus
ResponderExcluirMonique dos Santos Guerra
ResponderExcluirEduarda Santana Gonçalves
ResponderExcluirEdenilton de jesus Santos
ResponderExcluirNaiara Souza santos
ResponderExcluirAlfrânia Pereira santos
ResponderExcluir